Каждый день мы пользуемся какими-нибудь предметами: берем их в руки, совершаем над ними любые манипуляции - переворачиваем, рассматриваем, в конце концов, ломаем. А вы никогда не задумывались о том, из чего состоят эти предметы? "Чего уж здесь думать? Из металла/дерева/пластика/ткани!" - недоуменно ответят многие из нас. Отчасти это правильный ответ. А из чего состоят эти материалы - металл, дерево, пластик, ткань и многие другие вещества? Сегодня мы и обсудим этот вопрос.
Молекула и атом: определение
У знающего человека ответ на него прост и банален: из атомов и молекул. Но некоторые люди озадачиваются и начинают сыпать вопросами: "Что такое атом и молекула? Как они выглядят?" и т.д., и т.п. Ответим на эти вопросы по порядку. Ну, во-первых, что такое атом и молекула? Скажем вам сразу, что эти определения - не одно и то же. И даже более того - это совершенно разные термины. Итак, атом - это самая маленькая часть химического элемента, которая является носителем его свойств, частица вещества мизерных массы и размеров. А молекула - это электрически нейтральная частица, которую образуют несколько соединенных ковалентными связями атомов.
Что такое атом: строение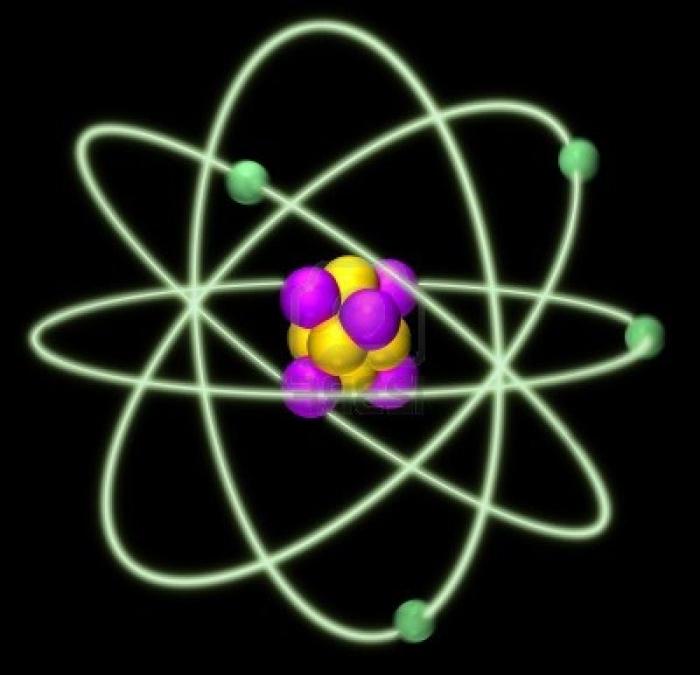
Атом состоит из электронной оболочки и атомного ядра (фото). В свою очередь ядро состоит из протонов и нейтронов, а оболочка - из электронов. В атоме протоны заряжены положительно, электроны - отрицательно, а нейтроны вообще не заряжены. Если число протонов соответствует количеству электронов, то атом является электронейтральным, т.е. если мы прикоснемся к веществу, образованному из молекул с такими атомами, то не почувствуем ни малейшего электрического импульса. И даже сверхмощные ЭВМ его не уловят по причине отсутствия последнего. Но случается так, что протонов больше, чем электронов, и наоборот. Тогда такие атомы правильнее будет называть ионами. Если в нем больше протонов, то он электрически положительный, если же преобладают электроны - электрически отрицательный. В каждом определенном атоме есть строгое количество протонов, нейтронов и электронов. И его можно высчитать. Шаблон для решения задач по нахождению количества этих частиц выглядит так:
Хим. элемент - R (вставить название элемента)Протоны (p) - ?Электроны (е) - ?Нейтроны (n) - ?Решение:р = порядковый № хим. элемента R в периодической системе им Д.И. Менделеевае = рn = Аr (R) - № R
Что такое молекула: строение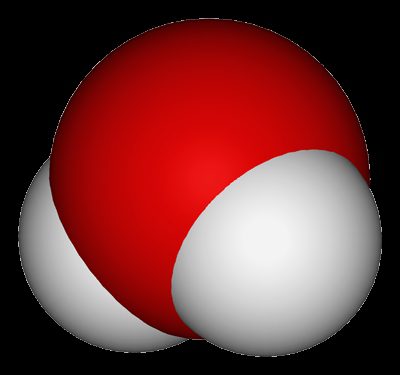
Молекула - это наименьшая частица химического вещества, то есть она уже непосредственно входит в его состав. Молекула определенного вещества состоит из нескольких одинаковых или различных атомов. Особенности строения молекул зависят от физических свойств вещества, в котором они присутствуют. Молекулы состоят из электронов и атомов. Расположение последних можно узнать с помощью структурной формулы. Строение молекулы позволяет определить ход химической реакции. Обычно они нейтральные (не имеют электрического заряда), и у них нет неспаренных электронов (все валентности являются насыщенными). Однако они могут быть и заряженными, тогда их правильное название - ионы. Также у молекул могут быть неспаренные электроны и ненасыщенные валентности - в этом случае их называют радикалами.
Заключение
 Теперь вы знаете, что такое атом и что такое молекула. Все без исключения вещества состоят из молекул, а последние, в свою очередь, построены из атомов. Физические свойства вещества определяют расположение и связь атомов и молекул в нем.
Теперь вы знаете, что такое атом и что такое молекула. Все без исключения вещества состоят из молекул, а последние, в свою очередь, построены из атомов. Физические свойства вещества определяют расположение и связь атомов и молекул в нем.
fb.ru
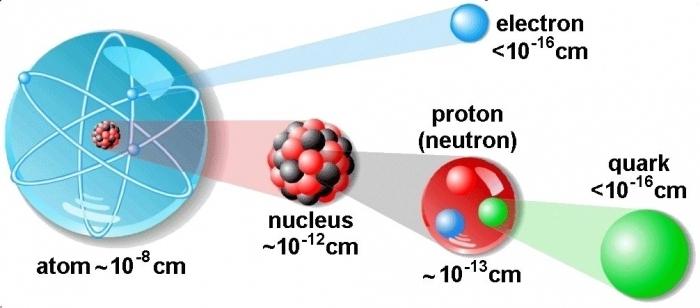
Атомы — это маленькие частицы, из которых состоит вещество. Невозможно даже представить себе, насколько они малы. Если сложить в цепочку сто миллионов атомов, у нас получится ниточка длиной всего лишь в 1 см. В тонком листе бумаги, наверное, не меньше миллиона слоев атомов. Науке известно более ста видов атомов; соединяясь друг с другом, они образуют все окружающие нас вещества.
Мысль о том, что всё в природе состоит из атомов, возникла давно. Еще 2500 лет назад древнегреческие философы полагали, что вещество состоит из таких частиц, которые нельзя разделить. Само слово «атом» восходит к греческому слову «атомос», что значит «неделимый». В Древней Греции (см. статью «Загадочные жители Греции«) философы обсуждали гипотезу о том, что всё вещество в мире состоит из неделимых частиц. Правда, Аристотель в этом сомневался.
Термин «атом» был впервые использован английским химиком Джоном Дальтоном (1766- 1844). В 1807 г. Дальтон выдвинул свою атомную теорию. Атомами он назвал составляющие всякое вещество малые частицы, которые не изменяются входе химических реакций. Согласно Дальтону, химическая реакция — это процесс, при котором атомы соединяются вместе или отделяются друг от друга. Атомная теория Дальтона лежит в основе представлений современных ученых.
В начале нашего столетия ученые начали строить модели атомов. Эрнест Резерфорд (1871 — 1937) показал, что отрицательно заряженные электроны обращаются вокруг положительно заряженного ядра. Нильс Бор (1885 — 1962) утверждал, что электроны обращаются по определенным орбитам. В 1932 г. Джеймс Чедвик (1891 — 1974) установил, что ядро атома состоит из частиц, которые он назвал протонами и нейтронами.
Атомы состоят из еще меньших, чем они сами, частиц, называемых элементарными. Центром атома является его ядро. Оно состоит из элементарных частиц двух видов — протонов и нейтронов. Есть в атоме также другие элементарные частицы — электроны; они вращаются вокруг ядра. Существует множество разных элементарных частиц. Ученые считают, что протоны и нейтроны состоят из кварков. Элементарные частицы, входящие в состав атома, удерживаются вместе благодаря своим электрическим зарядам. Протоны заряжены положительно, а электроны — отрицательно. Нейтроны заряда не имеют, т.е. являются электрически нейтральными. Частицы, несущие противоположные электрические заряды, притягиваются друг к другу. Притяжение отрицательно заряженных электронов к положительно заряженным протонам, находящимся в атомном ядре, удерживает электроны на орбитах около этого ядра. В состав атома входит одинаковое число положительно заряженных протонов и отрицательно заряженных электронов, и атом электрически нейтрален.Электроны в атоме находятся на разных энергетических уровнях, или оболочках. Каждая оболочка состоит из определенного числа электронов. Когда очередная оболочка заполняется, новые электроны попадают на следующую оболочку. Большую часть объема атома занимает пустое пространство между элементарными частицами. Отрицательно заряженные электроны удерживаются на своих энергетических уровнях силой притяжения к положительно заряженным протонам ядра.
Строение атома часто описывают строгой диаграммой, однако сегодня ученые полагают, что электроны существуют на своих орбитах в размытом состоянии. Это представление отражено на рисунке, где электронные орбиты представлены в виде «облаков». Так вы бы увидели молекулу под электронным микроскопом. Равными цветами показаны разные уровни плотности электронов. Бирюзовым цветом отмечена область наибольшей плотности.
Атомный номер — это число протонов в атомном ядре. Как правило, в состав атома входит одинаковое число протонов и электронов, поэтому по атомному номеру можно судить и о том, сколько в атоме электронов. В разных атомах содержится разное количество протонов. В ядре атома фосфора 15 протонов и 16 нейтронов, значит, его атомный номер 15. В ядре атома золота 79 протонов и 118 нейтронов: следовательно, атомный номер золота 79.
Чем больше протонов и нейтронов имеет атом, тем больше его масса (величина, показывающая количество вещества в составе атома). Сумму числа протонов и числа нейтронов мы называем атомной массой. Атомная масса фосфора — 31. При исчислении атомной массы электроны в расчет не принимаются, так как их масса ничтожно мала по сравнению с массой атома. Существует особый прибор — масс-спектрометр. Он позволяет определить для каждого данного атома его массу.
У большинства элементов существуют изотопы, атомы которых имеют несколько отличное строение. Количество протонов и электронов в атомах изотопов одного элемента всегда неизменно. Атомы изотопов различаются числом нейтронов в ядре. Следовательно, у всех изотопов одного элемента один и тот же атомный номер, но разная атомная масса. На этом рисунке вы видите три изотопа углерода. У изотопа С12 есть 6 нейтронов и 6 протонов. С13 имеет 7 нейтронов. В ядре изотопа С12 восемь нейтронов и 6 протонов.
Физические свойства изотопов различны, но они обладают одинаковыми химическими свойствами. Обычно большая часть атомов элемента (вещества, состоящего из атомов одного вида) принадлежит к одному изотопу, а другие изотопы встречаются в меньших количествах.
Атомы редко встречаются и свободном состоянии. Как правило, они связываются друг с другом и образуют молекулы либо другие, более массивные структуры. Молекула — это мельчайшая частица вещества, которая может существовать самостоятельно. Она состоит из атомов, удерживающихся вместе при помощи связей. Например, у молекулы воды два атома водорода связанны с атомом кислорода. Атомы удерживаются вместе благодаря электрическим зарядам частиц, из которых они состоят. Описывая строение молекул, ученые прибегают к помощи моделей. Как правило, они пользуются структурными и пространственными моделями. Структурные модели представляют связи, удерживающие атомы вместе, в виде палочек. В пространственных моделях атомы плотно соединены друг с другом. Конечно, модель не похожа на настоящую молекулу. Модели строятся для того, чтобы показать, из каких атомов та или иная молекула состоит.
Химическая формула вещества показывает, сколько атомов каких элементов входит в состав одной молекулы. Каждый атом обозначается символом. Как правило, в качестве символа выбирается первая буква английского, латинского или арабского названия элемента. Например, молекула углекислою газа состоит из двух атомов кислорода и одного атома углерода, поэтому формула углекислого газа СО2. Двойка Атомы обозначает число атомов кислорода в молекуле.
Этот опыт продемонстрирует вам, что молекулы вещества удерживаются вместе силами притяжения. Наполните стакан водой до краев. Осторожно опустите в стакан несколько монет. Вы увидите, что над краями стакана приподнялся водяной купол. Сила, притягивающая молекулы воды друг к другу, может удержать некоторое количество воды над краями стакана. Эта сила называется силой поверхностного натяжения.
www.polnaja-jenciklopedija.ru
Очень часто можно услышать мнение, что атом будучи составной частью молекулы, обладает теми же свойствами и имеет аналогичную структуру. Такая позиция лишь отчасти имеет право на существование, поскольку частицы имеют общие и отличительные признаки. Для начала достаточно рассмотреть свойства двух объектов, и на их основе делать дальнейшие выводы.
Атом можно рассматривать как элементарную частицу однородного вещества. Такое вещество, по определению, состоит только из одного химического элемента (С, N, O и другие с периодической таблицы Менделеева). Именно наименьшая часть таких элементов, которая может быть носителем их свойств, и называется атомом. Согласно последним современным представлениям, атом состоит из трех составляющих: протонов, нейтронов и электронов.
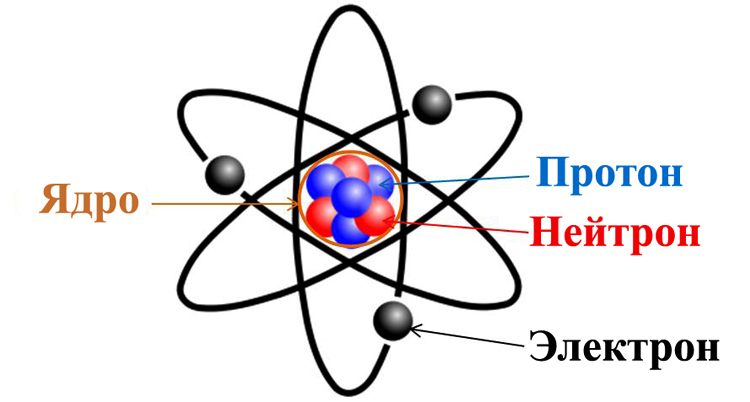
Атом
Первые две субчастицы вместе составляют базовое ядро, которое имеет положительный заряд. Двигающиеся вокруг ядра электроны привносят компенсационный заряд с противоположным знаком. Таким образом, делается первый вывод, что большинство атомов — электрически нейтральны. Что касается оставшейся части, то в силу различных физико-химических процессов, атомы могут либо присоединять, либо отпускать электроны, что приводит к появлению заряда. Атом имеет массу и размер (определяется размерами ядра) и определяет химические свойства вещества.
Молекула является минимальной структурной единицей вещества. Такое вещество может состоять из нескольких химических элементов. Однако, молекулой можно считать и одноатомное вещество одного химического элемента — инертный газ аргона. Как и атомы, является электрически нейтральной. Ионизировать молекулу можно, но уже значительно сложнее: атомы внутри молекулы связаны между собой ковалентной, либо ионной связью. Поэтому присоединить или забрать электрон становится значительно сложнее. Большинство молекул имеет сложную архитектурную постройку, где каждый атом заранее занимает отведенное ему место.
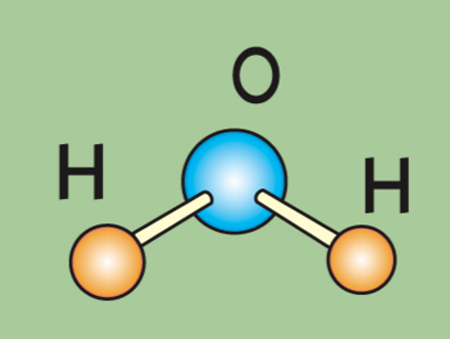
Строение молекулы воды
Строение. Обе частицы являются структурными единицами вещества. При этом под атомом подразумевается один определенный элемент, молекула же включает в себя уже несколько химически связанных атомов, но структура (положительное ядро с отрицательными электронами) остается той же.
Электрическая нейтральность. При отсутствии внешних факторов — взаимодействия с другим химическим веществом, направленного электрического поля и других раздражителей, — атомы и молекулы не имеют заряда.
Замещение. Атом может выступать как молекула в одном случае — при работе с инертными газами. Также молекулой может считаться одноатомная ртуть.
Наличие массы. Обе частицы имеют свою четкую массу. В случае атома масса зависит от химического элемента и определяется весом ядра (протон почти в 1500 раз тяжелее электрона, поэтому вес отрицательной частицы часто не берется во внимание). Масса молекулы определяется исходя из ее химической формулы — элементов, входящих в ее состав.
Неделимость. Атом является мельчайшим элементом, из которого нельзя выделить еще меньшую частицу. (Получение иона влияет только на заряд, но не на вес). Молекулу, в свою очередь, можно разделить на более мелкие молекулы или можно разложить на атомы. Процесса распада легко добиться с использованием химических катализаторов. Иногда достаточно просто нагреть вещество.
Свободное существование. Молекула может свободно существовать в природе. Атом существует в вольной форме лишь в двух случаях:
В остальных случаях атом всегда входит в состав молекулы.
Образование заряда. Взаимодействие между ядром и электроном в атоме можно легко преодолеть даже мельчайшим электрическим полем. Таким образом, — из атома легко получить положительный или отрицательный ион. Наличие химических связей между атомами внутри молекулы требует приложения гораздо большего электрического поля или взаимодействия с другим химически активным веществом.
vchemraznica.ru
Все вещества состоят из крошечных частиц - атомов. Атомы соединяются в молекулы, крупнейшие из которых имеют сложное строение, состоящее из тысяч атомов.
О том, что все сущее состоит из частиц, знали еще древние греки. Около 420 г. до н. э. философ Демокрит поддержал гипотезу, что материя состоит из крошечных, неделимых частиц. По-гречески atomos означает "неделимый", поэтому эти частицы назвали атомами.
Другие философы придерживались иной точки зрения, и в IV веке до н. э. Аристотель высказался в поддержку мнения, согласно которому материя состоит из различных сочетаний так называемых четырех стихий - земли, воздуха, огня и воды. Эта идея получила широкое распространение и легла в основу алхимии - примитивной формы химии, господствовавшей в науке до XVII века.
Одной из главных задач алхимии было создание "эликсира жизни" - снадобья, которое позволило бы человеку жить вечно. Другая заключалась в создании богатств путем превращения обычных металлов в золото. Многие алхимики утверждали, что решили эти задачи, однако никто из них так и не добился реального успеха.
Переворот в науке
Некоторые ученые продолжали придерживаться мнения, что материя состоит из атомов, но только в начале XIX века были получены экспериментальные данные, подтверждающие эту теорию. Английский химик и писатель Джон Дальтон проводил опыты с газами и изучал пути их соединения. Так, он обнаружил, что кислород и водород, образуя воду, всегда соединяются в одних и тех же пропорциях по массе. Другие ученые также сталкивались с подобными данными, но именно Дальтон впервые осознал их значение. Он сделал вывод, что вещества состоят из атомов, и что все атомы простого вещества имеют одинаковую массу. При соединении простых веществ количества соединяющихся атомов находятся в определенной неизменной пропорции. Атомистика Дальтона объясняла, почему вещества соединяются в неизменной массовой пропорции, а также явилась основой для детального изучения материи. Вещества состоят из атомов, а из чего состоят атомы? Первые ключи к разгадке этой тайны появились в конце XIX века, когда исследователи изучали прохождение электричества через разрядные трубки, содержащие разреженный воздух. Иногда стенки трубки излучали зеленый свет при подаче высокого напряжения на две металлические пластины - электроды. Свечение возникало при попадании невидимых лучей от отрицательного электрода, или катода, на стенки трубки.
В 1890-х годах английский физик Дж. Томсон доказал, что эти катодные лучи (как их тогда называли) - не что иное, как потоки отрицательно заряженных частиц. Предполагалось, что эти частицы исходят из атомов, хотя их расположение внутри атомов оставалось неясным. Томсон высказал предположение, что атом может быть похож на рождественский пудинг, в котором большая, но легкая по массе положительно заряженная сфера усеяна многочисленными отрицательно заряженными частицами (электронами). Однако различные опыты по изучению строения атома доказали, что это - безусловно ошибочная теория.
Строение атома
В 1911 году Эрнест Резерфорд, британский физик, уроженец Новой Зеландии, работавший вместе с Томсоном, предложил строение атома, реально объясняющее его поведение во время экспериментов. Резерфорд предположил, что центр (или ядро) атома имеет положительный заряд и относительно большую массу, а вокруг ядра вращаются крайне легкие и отрицательно заряженные электроны.
Однако Резерфорд не осознавал, что обычно в ядре атома находятся как положительно заряженные, так и нейтральные частицы. Существование положительно заряженных частиц было признано в 1920 г., и они получили название протоны. В 1932 г. английский физик Джеймс Чэдвик открыл незаряженные частицы и назвал их нейтронами. В результате картина строения атома была завершена и с тех пор является основой нашего понимания материи.
Элементы
Любое вещество, в котором все атомы имеют одинаковое количество протонов, называется элементом. Число протонов в каждом атоме - атомный номер элемента. Существуют 92 природных элемента, их атомы имеют от 1 до 92 протонов. Кроме того, некоторые другие элементы с еще большим числом протонов в атоме можно получить с помощью устройства под названием ускоритель элементарных частиц. К природным элементам относятся железо, ртуть и водород.
Во многих веществах атомы объединяются в группы, называемые молекулами. Так, газ водород состоит из молекул, каждая из которых содержит два атома водорода. Часто, однако, молекулы вещества состоят из атомов более одного элемента. Такие вещества называются соединениями. Например, вода является соединением, где каждая молекула состоит из двух атомов водорода и одного атома кислорода. Во многих молекулах насчитывается гораздо большее количество атомов. Некоторые белковые молекулы представляют собой сложные соединения из нескольких тысяч атомов. Некоторые природные элементы встречаются только в соединениях. Так, натрий - это металл, настолько легко соединяющийся с другими веществами, что его нельзя обнаружить в чистом виде. Он широко известен в сочетании с хлором в виде хлорида натрия - поваренной соли.
Связи
Атомы в молекулах связываются различными путями, при этом они разделяют между собой электроны или обмениваются ими. Двумя простыми видами химической связи являются ковалентная и ионная.
Ковалентная связь возникает, когда атомы имеют общие электроны. Так, молекула водородного газа состоит из двух атомов водорода, связанных ковалентной связью. Единственный электрон каждого атома водорода вращается вокруг ядер обоих атомов, связывая их воедино.
В случае ионной связи один атом передает электроны другому атому. В результате возникает электрическая сила, связывающая атомы воедино. Как правило, количество положительно заряженных протонов и отрицательно заряженных электронов в атоме одинаково. Их положительные и отрицательные заряды уравновешивают друг друга, и поэтому атом не имеет общего заряда. Однако в атоме, отдающем электроны, создается избыток положительного заряда, а атом, получающий электроны, приобретает общий отрицательный заряд. Такие заряженные атомы называются ионами. Ионы противоположных зарядов притягиваются друг к другу, и именно это электрическое притяжение удерживает атомы вместе при ионной связи. Например, молекула поваренной соли формируется с помощью ионной связи, когда атом натрия передает электрон атому хлора.
Все атомы одного вещества имеют одинаковое количество протонов, но различное количество нейтронов. Так, в углероде ядро большинства атомов содержит шесть нейтронов, но примерно в каждом сотом из них имеется семь нейтронов. Эти различные типы атомов одного и того же элемента называются изотопами. Все изотопы данного элемента обладают одинаковыми химическими свойствами - все они соединяются с другими веществами и образуют одни и те же химические соединения. Но отдельные физические свойства изотопов различаются - например, они имеют разные точки замерзания или кипения.
Говоря о конкретном изотопе того или иного элемента, ученые называют его массовое число. Например, углерод-12 - это обычный природный изотоп углерода. Его атом содержит шесть протонов и шесть нейтронов. Более редкий природный изотоп, в ядре каждого атома которого находится лишний нейтрон, называется углерод-13.
Атомный вес
Протон и нейтрон имеют почти одинаковую массу, которая более чем в 1800 раз превышает массу электрона. Поэтому когда речь идет о массе атома, как правило, не будет ошибкой ссылаться на его массовое число.
Атомный вес элемента, или его относительная атомная масса, обычно представляет собой среднюю массу смеси изотопов, встречающихся в природе. Молекулярный вес вещества, или его относительная молекулярная масса, - это сумма атомных весов всех атомов в одной молекуле данного вещества.
Многосложный атом
С тех пор экспериментировавшие с ускорителями ученые открыли сотни других видов частиц в атомах. Но, к счастью, простая модель атома достаточна для того, чтобы объяснить большую часть свойств материи.
mirznanii.com
Гипотеза о том, что все вещества состоят из отдельных мельчайших частиц, появилась очень давно, более двух тысяч лет назад. Но лишь на рубеже XIX — XX вв. было установлено, что это за частицы и какими свойствами они обладают.
Частицы, из которых состоят вещества, называют молекулами. Так, например, наименьшая частица воды — это молекула воды, наименьшая частица сахара — это молекула сахара и т. д.
Каковы размеры молекул?
Известно, что кусок сахара можно растолочь на очень маленькие крупинки, зерно пшеницы можно размолоть в муку. Капля масла, растекаясь по поверхности воды, может образовать пленку, толщина которой в десятки тысяч раз меньше диаметра человеческого волоса. Но в крупинке муки и в толще масляной пленки содержится не одна, а много молекул. Значит, размеры молекул этих веществ еще меньше, чем размеры крупинки муки и толщина пленки.
Можно привести следующее сравнение: молекула во столько же раз меньше яблока среднего размера, во сколько раз яблоко меньше земного шара. Если бы размеры всех тел увеличились в миллион раз (при этом толщина человеческого пальца стала бы равной 10 км), то и тогда молекула оказалась бы размером всего вполовину точки печатного шрифта этого учебника.
Молекулы невозможно увидеть невооруженным глазом. Они настолько малы, что их нельзя разглядеть даже с помощью микроскопа, дающего 1000-кратное увеличение.
Биологам известны микроорганизмы (например, бактерии) размером 0,001 мм. Молекулы же в сотни и тысячи раз меньше.
Для определения размеров молекул были проведены разные опыты. Опишем один из них.
В чисто вымытый большой сосуд налили воду и на ее поверхность поместили каплю масла. Масло начало растекаться по поверхности воды, образуя пленку. По мере растекания масла толщина пленки становилась все меньше и меньше. Через некоторое время растекание прекратилось. Если предположить, что это произошло из-за того, что все молекулы масла оказались на поверхности воды (образуя пленку толщиной в одну молекулу), то для определения диаметра молекулы достаточно найти толщину образовавшейся пленки.
Толщина пленки h равна отношению ее объема V к площади S:
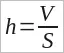 (26.1)
(26.1)
Объем пленки — это объем той капли, которую поместили на поверхность воды. Его измеряют заранее; для этого пользуются измерительным цилиндром — мензуркой. При помощи пипетки в пустую мензурку капают несколько десятков капель масла и измеряют их общий объем; разделив затем этот объем на число капель, находят объем одной капли.
В описываемом опыте капля имела объем V = 0,0009 см3, а площадь образовавшейся из нее пленки была равна S = 5500 см2. Подставив эти значения в формулу (26.1), получим
h = 0,00000016 см.
Этим числом и выражается примерный размер молекулы масла.
Так как молекулы очень малы, то в каждом теле их содержится огромное количество. Чтобы создать представление об их числе, приведем пример: если в детском резиновом шарике, наполненном водородом, сделать такой тонкий прокол, что из него каждую секунду будет выходить по миллиону молекул, то для вылета всех молекул из шарика понадобится 30 миллиардов лет! И это при том, что масса водорода, наполнявшего шарик, составляла всего 3 г.
Хотя молекулы и очень маленькие частицы, но и они делимы. Частицы, из которых состоят молекулы, называют атомами.
Атомы каждого вида принято обозначать специальными символами. Например:
атом кислорода — О,атом водорода — Н,атом углерода — С.
Специальные символы (так называемые химические формулы) существуют и для обозначения молекул. Например, молекула кислорода состоит из двух одинаковых атомов кислорода, поэтому для ее обозначения применяют следующую химическую формулу: O2. Молекула воды состоит из трех атомов: одного атома кислорода и двух атомов водорода, поэтому ее обозначают h3O.
На рисунке 68 дано условное изображение двух молекул воды. При делении двух молекул воды получаются два атома кислорода и четыре атома водорода. Каждые два атома водорода могут объединиться в молекулу водорода, а атомы кислорода — в молекулу кислорода, что схематически показано на рисунке 69. Современная техника позволяет получить фотографии отдельных атомов и молекул. На рисунке 70 приведен снимок молекулы фторида мышьяка, полученный с помощью электронно-голографического микроскопа, дающего увеличение в 70 миллионов раз. Фотографию отдельного атома можно увидеть на рисунке 71, это изображение атома аргона, увеличенное в 260 миллионов раз.
Современная техника позволяет получить фотографии отдельных атомов и молекул. На рисунке 70 приведен снимок молекулы фторида мышьяка, полученный с помощью электронно-голографического микроскопа, дающего увеличение в 70 миллионов раз. Фотографию отдельного атома можно увидеть на рисунке 71, это изображение атома аргона, увеличенное в 260 миллионов раз.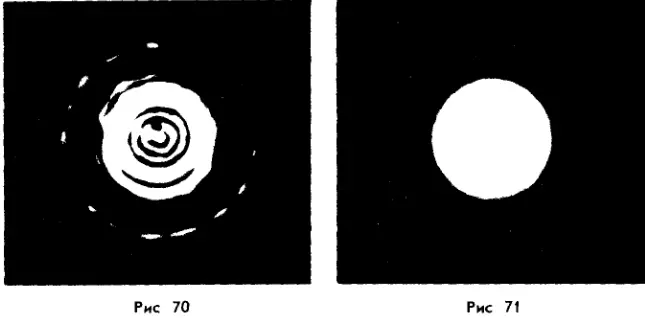 Атомы очень маленькие частицы, но и они имеют сложное строение. Существуют еще более мелкие частицы, о которых вы узнаете позже.
Атомы очень маленькие частицы, но и они имеют сложное строение. Существуют еще более мелкие частицы, о которых вы узнаете позже.
1. Как называются частицы, из которых состоят вещества? 2. Опишите опыт, с помощью которого можно определить размер молекулы. 3. Как называются частицы, из которых состоят молекулы? 4. Из каких атомов состоит молекула воды? Что означает формула Н2О? 5. Напишите химическую формулу молекулы водорода, если известно, что эта молекула состоит из двух одинаковых атомов водорода. 6. Из скольких (и каких) атомов состоит молекула углекислого газа, если ее химическая формула имеет вид СO2?
phscs.ru
Ключевые слова конспекта: Атомно-молекулярное учение, атомы, молекулы и ионы, элементарные частицы, ядро, электрон, протон, нейтрон.
Древнегреческий философ Демокрит 2500 лет назад предположил, что все тела состоят из мельчайших, невидимых, неделимых, вечно движущихся частиц — атомов. В переводе «атом» означает «неделимый».
Учение о молекулах и атомах в основном было разработано в XVIII— XIX вв. Великий русский учёный М. В. Ломоносов утверждал, что тела в природе состоят из корпускул (молекул), в состав которых входят элементы (атомы). Многообразие веществ учёный объяснял соединением разных атомов в молекулах и различным расположением атомов в них.

Основоположником атомно-молекулярного учения принято считать известного английского учёного Джона Дальтона. Тем не менее некоторые представления об атомах и молекулах, высказанные Ломоносовым за полвека до Дальтона, оказались более достоверными, научными. Например, английский учёный отрицал возможность существования молекул, образованных одинаковыми атомами.
Атомно-молекулярное учение получило окончательное признание только в 1860 г. на Всемирном съезде химиков в Карлсруэ.
Каждое отдельно взятое вещество состоит из одинаковых молекул. Например, вещество вода состоит из молекул воды. Но размеры молекул воды очень малы, поэтому даже маленькая капелька воды содержит огромное количество молекул, которые имеют одинаковые состав и свойства.
Молекулы — это мельчайшие частицы многих веществ, состав и химические свойства которых такие же, как у данного вещества. При химических реакциях молекулы распадаются, то есть они являются химически делимыми частицами. Молекулы состоят из атомов.

Следует иметь в виду, что существуют также вещества, состоящие из отдельных одинаковых атомов. Мельчайшими частицами, сохраняющими характерные химические свойства таких веществ, являются атомы. Так, из отдельных атомов состоят благородные газы — гелий, неон, аргон и др. Атомы в отличие от молекул в ходе химических реакций не делятся на более мелкие части.
Атомы — это мельчайшие химически неделимые частицы вещества.
В конце XIX—начале XX в. было обнаружено, что атомы состоят из ешё более мелких частиц. Эти частицы были названы элементарными частицами. В центре атома находится положительно заряженное ядро, вокруг которого находятся отрицательно заряженные частицы — электроны. Заряд электрона принято считать равным —1.
Ядро атома, в свою очередь, также состоит из элементарных частиц. В состав ядер атомов входят положительно заряженные частицы — протоны и частицы, имеющие почти такую же массу, как протоны, но не имеющие заряда,— нейтроны. Заряд протона численно равен заряду электрона, но имеет противоположный знак (+1).
Например, атом водорода состоит из ядра, в котором находится только один протон и один электрон. Атом гелия состоит из ядра, в котором находятся 2 протона и 2 нейтрона, а также 2 электрона. Атом лития состоит из ядра, в котором находятся 3 протона, 4 нейтрона, а также 3 электрона.
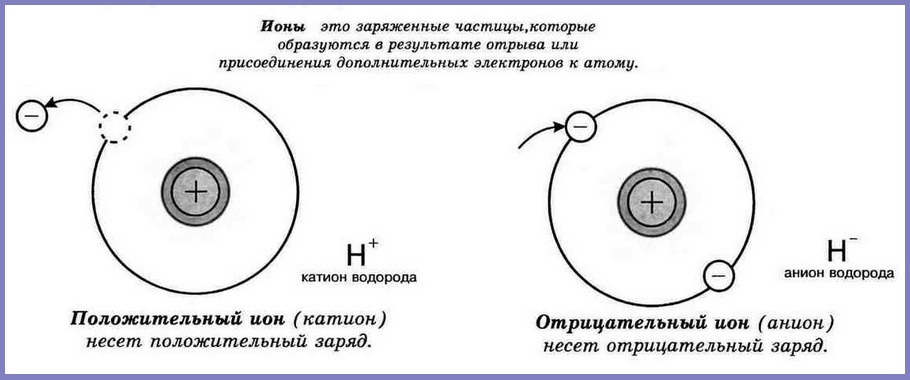
Одни атомы, взаимодействуя с другими атомами, могут терять или, наоборот, приобретать один или более электронов. В результате электрически нейтральный атом превращается в заряженную частицу — ион. Если атом теряет один или несколько электронов, его называют положительно заряженным ионом. Атом, дополнительно присоединивший один или несколько электронов, называют отрицательно заряженным ионом. Противоположно заряженные ионы притягиваются друг к другу. Подробнее электронно-ионная теория рассматривается в курсе физики (читать Конспект «Электронно-ионная теория»)
Конспект урока «Атомы, молекулы и ионы».
Следующая тема: «Простые и сложные вещества».
Атомы, молекулы и ионы
5 (100%) 1 voteuchitel.pro
Еще много веков назад люди догадывались, что любое вещество на земле состоит из микроскопических частиц. Прошло какое-то время, и ученые доказали, что эти частицы действительно существуют. Их назвали атомами. Обычно атомы не могут существовать отдельно и объединяются в группы. Эти группы и называются молекулами.  Само название "молекула" происходит от латинского слова moles, означающего тяжесть, глыбу, громаду, и уменьшительного суффикса – cula. Раньше вместо этого термина употреблялось слово «корпускула», дословно означающее «маленькое тело». Для того чтобы выяснить, что такое молекула, обратимся к толковым словарям. В словаре Ушакова говорится, что это мельчайшая частица, которая может существовать автономно и обладает всеми свойствами вещества, к которому она относится. Молекулы и атомы окружают нас повсюду, и хоть их нельзя пощупать, все, что мы видим, на самом деле - это их гигантские скопления.
Само название "молекула" происходит от латинского слова moles, означающего тяжесть, глыбу, громаду, и уменьшительного суффикса – cula. Раньше вместо этого термина употреблялось слово «корпускула», дословно означающее «маленькое тело». Для того чтобы выяснить, что такое молекула, обратимся к толковым словарям. В словаре Ушакова говорится, что это мельчайшая частица, которая может существовать автономно и обладает всеми свойствами вещества, к которому она относится. Молекулы и атомы окружают нас повсюду, и хоть их нельзя пощупать, все, что мы видим, на самом деле - это их гигантские скопления.
Пример с водой
Лучше всего объяснить, что такое молекула, можно на примере стакана с водой. Если отлить из него половину, то вкус, цвет и состав оставшейся воды не изменится. Было бы странно ожидать чего-то другого. Если снова отлить половину, количество уменьшится, но свойства опять останутся теми же. Продолжая в том же духе, мы в итоге получим маленькую капельку. Ее еще можно поделить пипеткой, но до бесконечности продолжать этот процесс не получится. 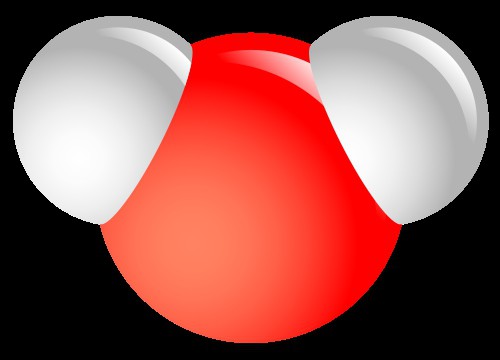 В конечном счете получится мельчайшая частица, остаток от деления которой водой уже не будет. Для того чтобы представить себе, что такое молекула и насколько она мала, попробуйте угадать, сколько молекул находится в одной капельке воды. Как вы думаете? Миллиард? Сто миллиардов? На самом деле их там примерно сто секстильонов. Это число, у которого после единицы идет двадцать три нуля. Такую величину сложно себе представить, поэтому воспользуемся сравнением: размер одной молекулы воды меньше крупного яблока во столько раз, во сколько само яблоко меньше земного шара. Поэтому ее нельзя увидеть даже в самый мощный оптический микроскоп.
В конечном счете получится мельчайшая частица, остаток от деления которой водой уже не будет. Для того чтобы представить себе, что такое молекула и насколько она мала, попробуйте угадать, сколько молекул находится в одной капельке воды. Как вы думаете? Миллиард? Сто миллиардов? На самом деле их там примерно сто секстильонов. Это число, у которого после единицы идет двадцать три нуля. Такую величину сложно себе представить, поэтому воспользуемся сравнением: размер одной молекулы воды меньше крупного яблока во столько раз, во сколько само яблоко меньше земного шара. Поэтому ее нельзя увидеть даже в самый мощный оптический микроскоп.
Строение молекул и атомов
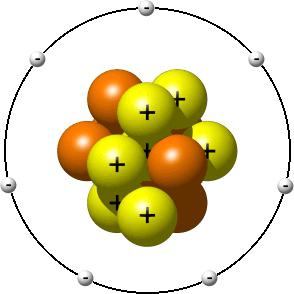 Как мы уже знаем, все микроскопические частицы в свою очередь состоят из атомов. В зависимости от их количества, орбит центральных атомов и типа связей геометрическая форма молекул может быть различной. К примеру, человеческая ДНК закручена в форме спирали, а мельчайшая частица обычной поваренной соли имеет вид кристаллической решетки. Если у молекулы каким-то образом забрать несколько атомов, произойдет ее разрушение. При этом последние никуда не денутся, а войдут в состав другой микрочастицы.
Как мы уже знаем, все микроскопические частицы в свою очередь состоят из атомов. В зависимости от их количества, орбит центральных атомов и типа связей геометрическая форма молекул может быть различной. К примеру, человеческая ДНК закручена в форме спирали, а мельчайшая частица обычной поваренной соли имеет вид кристаллической решетки. Если у молекулы каким-то образом забрать несколько атомов, произойдет ее разрушение. При этом последние никуда не денутся, а войдут в состав другой микрочастицы.
После того как мы разобрались, что такое молекула, перейдем к атому. Его структура очень напоминает планетарную систему: в центре находится ядро с нейтронами и положительно заряженными протонами, а вокруг на разных орбитах вращаются электроны. В целом атом электронейтрален. Другими словами, число электронов равно числу протонов.
Надеемся, наша статья оказалась полезной, и теперь у вас больше нет вопросов о том, что такое молекула и атом, как они устроены и чем отличаются.
fb.ru